L'atome
L’atome est composé d’un noyau central, entouré d’un nuage électronique.
1./ Le noyau atomique :
Le noyau se trouve au centre de l’atome. Il est formé de particules appelées nucléons. Il y a deux types de nucléons : les protons, chargés positivement et les neutrons, électriquement neutres. Un noyau atomique particulier est désigné par une notation symbolique qui indique la composition et la nature de ce noyau :

Lorsqu’on connaît le numéro atomique Z et le nombre de masse A, on obtient facilement le nombre de neutrons dans le noyau : A – Z.
2./ Le nuage (ou cortège) électronique :
Autour du noyau de l’atome tournent des électrons (e-), petites particules chargées négativement. Ces électrons sont en mouvement très rapides autour du noyau et on ne peut pas définir précisément leurs trajectoires. On ne peut que calculer la probabilité de trouver un électron en un point donné. On appelle nuage électronique la zone chargée négativement entourant le noyau et contenant les électrons. Il y a autant d’électrons dans le nuage électronique que de protons dans le noyau, soit Z.
3./ Caractéristiques de l’atome :
Le noyau de l’atome peut être considéré comme une sphère d’un rayon d’environ 10–15 m, soit 1 fm. Le nuage électronique peut être considéré comme une sphère d’un rayon d’environ 10–10 m, soit 100 pm. Le noyau est donc environ 100 000 fois plus petit (10–10 / 10–15) que l’atome. L’atome est donc essentiellement constitué de vide : on dit que l’atome a une structure lacunaire.
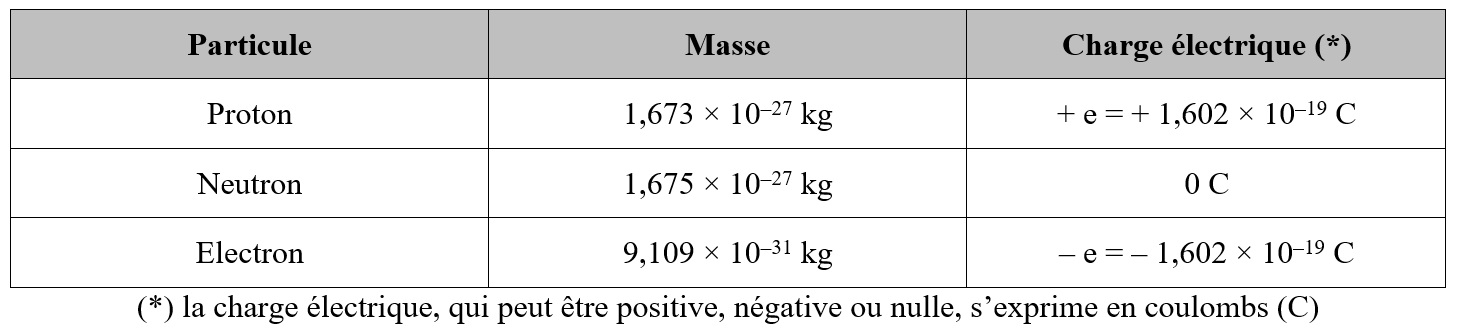
Remarques :
- On peut voir que la masse du proton (mproton) est presque égale à celle du neutron (mneutron). Pour simplifier les calculs, on peut considérer que tous les nucléons ont la même masse : mnucléon = 1,67 × 10–27
- La masse d’un nucléon est beaucoup plus grande que la masse de l’électron : mnucléon ≈ 2000 × mélectron. Il en résulte que pratiquement toute la masse de l’atome est concentrée dans le noyau de celui-ci.
- La charge électrique du proton, qui est aussi celle de l’électron, au signe près, est aussi appelé la charge électrique élémentaire. On la note « e ».
Un atome possédant autant d’électrons que de protons dans le noyau, et les charges du proton et de l’électron étant opposées, un atome porte une charge électrique nulle : on dit que l’atome est électriquement neutre.
La masse d’un atome étant pratiquement égale à celle du noyau, on peut calculer la masse d’un atome avec la formule suivante :
matome = A × mnucléon
L'élément chimique
1./ Définition :
Un élément chimique est défini par son numéro atomique Z, c’est-à-dire par le nombre de protons du noyau. Par exemple, un atome ou un ion ayant 29 protons dans le noyau est un représentant de l’élément cuivre, quel que soit le composé dont il fait partie.
2./ Isotopes :
Tous les atomes d’un même élément ont, par définition, le même nombre de protons dans leur noyau. Par contre, ils peuvent avoir un nombre de neutrons différents.

Lors d’une réaction chimique, la structure du noyau (nombre de protons et nombre de neutrons) ne sera JAMAIS modifiée. (Le rêve des alchimistes de fabriquer de l’or par voie chimique est donc impossible à réaliser). Seul le nuage électronique (nombre d’e–) pourra subir une modification.
Structure électronique de l'atome
1./ Une structure « en couches » :
Les Z e– du nuage électronique d’un atome sont liés au noyau par l’attraction des Z protons du noyau (les charges positives et négatives s’attirent). Pour arracher les e– de l’attraction du noyau, il faut leur fournir de l’énergie. L’expérience montre que certains e– sont plus faciles à arracher que d’autres : ils sont moins liés au noyau. Les e– sont donc répartis en couches électroniques : dans une même couche électronique sont regroupés tous les e– nécessitant la même énergie d’extraction. C’est pour cela que l’on utilise aussi l’expression niveaux d’énergie. Les e– d’une même couche sont en moyenne à la même distance du noyau.
2./ Comment nomme-t-on les couches électroniques ?
Chaque couche électronique est caractérisée par un nombre entier n ≥ 1, appelé nombre quantique principal. Les couches électroniques peuvent se découper en sous-couches. On introduit alors un nombre entier l tel que 0 ≤ l < n. Ce nombre l est appelé nombre quantique azimutal. Si l = 0, on parle de la sous-couche « s » ; si l = 1, on parle de la sous-couche « p », si l = 2, on parle de la sous-couche « d », si l = 3, on parle de la sous-couche « f », …
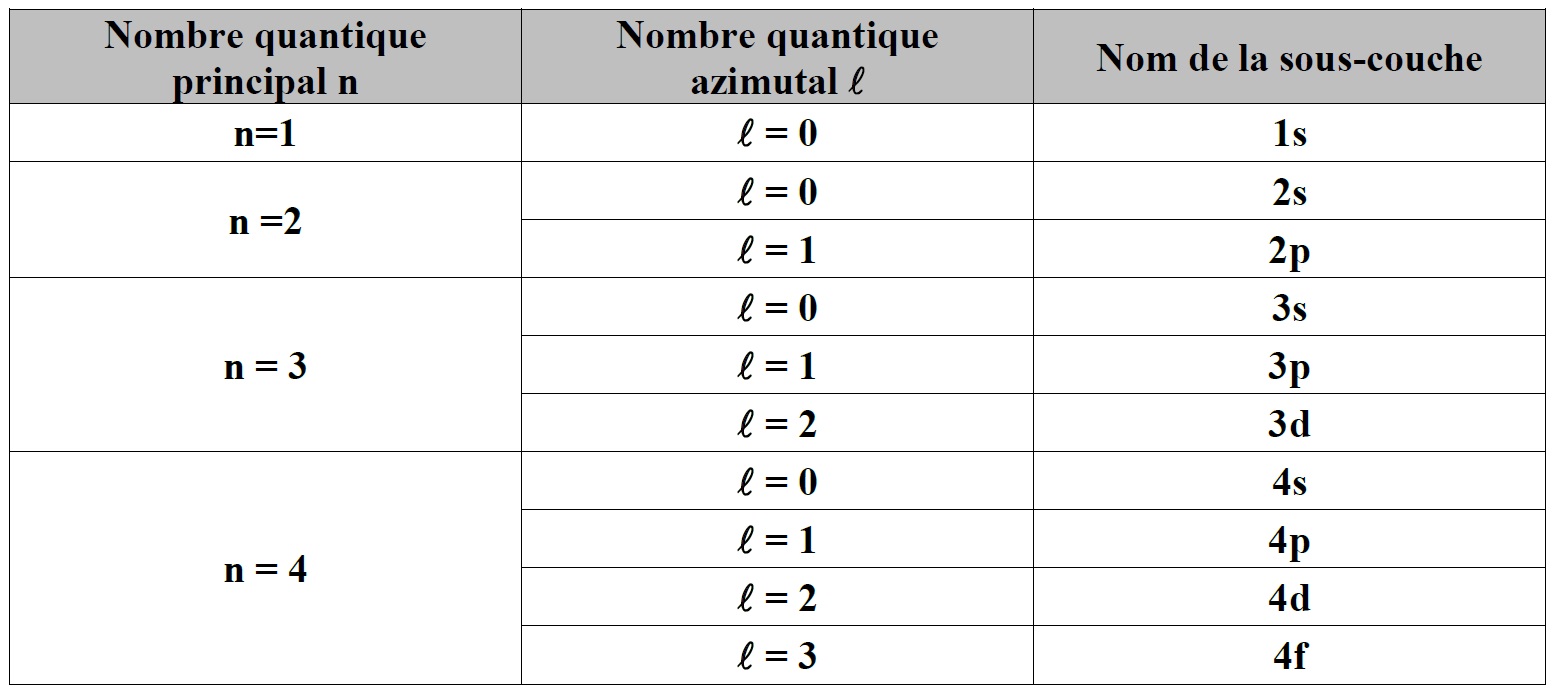
3./ Remplissage des couches électroniques :
Les e– vont se répartir dans les différentes couches et sous-couches électroniques en suivant les règles de remplissage suivantes :

Exemples : Carbone (Z = 6) : structure électronique (ou configuration électronique) : 1s2 2s2 2p4 ; Phosphore (Z = 15) : 1s2 2s2 2p6 3s2 3p3 ; Hélium (Z = 2) : 1s2 ; …
Remarques :
- Il ne faut savoir établir la structure électronique que pour les éléments de numéro atomique compris entre 1 et 18.
- Pour les éléments de numéro atomique supérieur à 18, il peut exister des irrégularités de remplissage pour des raisons qui ne sont pas au programme.

Exemple : l’aluminium Al a un numéro atomique égal à 13. Sa structure électronique est : 1s2 2s2 2p63s2 3p1.
1s2 2s2 2p6 : couches internes. Elles contiennent 10 e– de cœur.
3s2 3p1 : couche externe. Elle contient 3 e– de valence.
Classification périodique des éléments
Les éléments chimiques sont classés par ordre de numéro atomique croissant. Chaque ligne horizontale, appelée période, correspond au remplissage partiel ou total d’une couche électronique. Une nouvelle ligne est créée lorsqu’une nouvelle couche commence à se remplir. Examinons les trois premières périodes :
1./ première période :
La première couche électronique (n = 1) ne peut contenir que 2 e-. Il n’y a donc que deux éléments dans cette période : l’hydrogène H de structure électronique 1s1 et l’hélium He de structure électronique 1s2.

2./ deuxième période :
La deuxième période correspond au remplissage de la deuxième couche électronique (n = 2). Celle-ci pouvant contenir 8 e-, la deuxième période comporte 8 éléments :

3./ troisième période :
Elle correspond au remplissage partiel de la couche électronique (n = 3). Elle comporte 8 éléments. La fin du remplissage de la couche (n = 3) se fait à la période suivante.
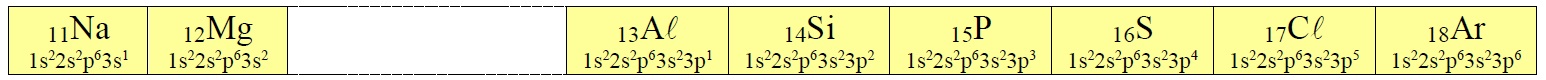
Moyen mnémotechnique pour se rappeler les périodes 2 et 3 :
Lili Berce Bébé Car Notre Oncle Fume Nerveusement
Napoléon Mangea Allègrement Six Poulets Sans Claquer Après
On remarque que dans une même colonne (appelée famille chimique), les atomes ont le même nombre d’e– sur leur couche externe. Dans une même famille, les atomes ont des propriétés chimiques très voisines.
Quelques familles notables :
- Première colonne : (sauf H) famille des métaux alcalins.
- Avant dernière colonne : famille des halogènes.
- Dernière colonne : famille des gaz nobles (ou gaz inertes, ou gaz rares).