Certaines réactions chimiques impliquent le transfert d'un ou de plusieurs électrons d'un premier réactif vers un deuxième réactif. Ces réactions sont appelés réactions d'oxydo-réduction.
Couple oxydant-réducteur
Un oxydant est une espèce chimique susceptible de capter un ou plusieurs électrons. On dit qu'il subit une réduction, ou qu'il est réduit.
⇒ La réduction d'une espèce chimique correspond donc à un gain d'électron(s) par cette espèce chimique.
Exemples : l'ion cuivre II Cu2+ est un oxydant. Dans certaines conditions, il peut capter deux électrons selon l'équation suivante : Cu2+ + 2 e- → Cu
Un réducteur est une espèce chimique susceptible de perdre un ou plusieurs électrons. On dit qu'il subit une oxydation, ou qu'il est oxydé.
⇒ L'oxydation d'une espèce chimique correspond donc à une perte d'électron(s) par cette espèce chimique.
Exemple : l'atome de cuivre Cu est un réducteur. Dans certaines conditions, il peut perdre deux électrons selon l'équation suivantes : Cu → Cu2+ + 2 e-
Un couple oxydant / réducteur (appelé aussi couple rédox) est formé d'un oxydant et d'un réducteur conjugués. Ces deux espèces chimiques sont liées dans la demi-équation électronique suivante :
oxydant + n e- = réducteur
Exemple : comme on l'a vu précédemment, Cu2+ et Cu sont associés et font partie du couple oxydant / réducteur Cu2+/Cu. La demi-équation électronique qui lie ces deux espèces chimiques est :
Cu2+ + 2 e- = Cu
Ecriture et équilibrage des demi-équations électroniques
La demi-équation électronique de certains couples oxydant / réducteur sont très simples à écrire et à équilibrer, comme c'est le cas pour l'exemple du couple Cu2+/Cu. Mais pour d'autres couples, il faut des étapes supplémentaires :
- Ecrire l'oxydant et le réducteur de part et d'autres du signe =
- Equilibrer les atomes autres que H et O s'il y en a
- Ajouter des molécules d'eau H2O pour équilibrer les atomes d'oxygène O
- Ajouter des ions H+ pour équilibrer les atomes d'hydrogène H
- Ajouter des e- pour équilibrer les charges électriques
Premier exemple : couple (Al3+/Al) :
- Al3+ = Al
- Les atomes d'aluminium Al sont déjà équilibrés.
- Pas d'atomes d'oxygène O.
- Pas d'atomes d'hydrogène H.
- Al3+ + 3 e- = Al
Deuxième exemple : couple (O2/H2O2) :
- O2 = H2O2
- Pas d'autres atomes que H et O.
- Les atomes d'oxygène O sont déjà équilibrés.
- O2 + 2 H+ = H2O2
- O2 + 2 H+ + 2 e- = H2O2
Troisième exemple : couple (Cr2O72-/Cr3+) :
- Cr2O72- = Cr3+
- Cr2O72- = 2 Cr3+
- Cr2O72- = 2 Cr3+ + 7 H2O
- Cr2O72- + 14 H+ = 2 Cr3+ + 7 H2O
- Cr2O72- + 14 H+ + 6 e- = 2 Cr3+ + 7 H2O
Equation d'une réaction d'oxydo-réduction
Une réaction d'oxydo-réduction implique un transfert d'électrons entre le réducteur d'un premier couple et l'oxydant d'un deuxième couple.
Pour pouvoir écrire et équilibrer une réaction d'oxydo-réduction, il faut suivre la méthode suivante :
- Ecrire la demi-équation de chaque couple mis en jeu, en mettant le réactif à gauche.
- Multiplier les demi-équations électroniques par un nombre entier de façon à ce qu'elles aient le même nombre d'électrons.
- Additionner les demi-équations électroniques membre à membre.
- Simplifier si besoin.
Important : il ne faut pas que des électrons apparaissent dans la réaction d'oxydo-réduction.
Premier exemple : Les ions hypochlorite ClO- réagissent avec les ions fer II Fe2+ pour former du dichlore Cl2 et des ions fer III Fe3+.
Les deux couples rédox mis en jeu sont : ClO-/Cl2 et Fe3+/Fe2+
On applique alors la méthode précédente :
- Les réactifs sont les ions ClO- et Fe2+. On écrit et on équilibre donc les deux demi-équations électroniques dans le bon sens, avec le réactif à gauche :
2 ClO- + 4 H+ + 4 e- = Cl2 + 2 H2O
Fe2+ = Fe3+ + e- - On remarque que le nombre d'électrons mis en jeu dans chacune de ces deux demi-équations électroniques n'est pas le même : il y en a 4 dans la première, et 1 dans la deuxième. On va donc multiplier la première par 1 et la deuxième par 4 (car 4 × 1 = 1 × 4 = 4) :
2 ClO- + 4 H+ + 4 e- = Cl2 + 2 H2O
4 Fe2+ = 4 Fe3+ + 4 e- - On additionne les deux demi-équations électroniques membre à membre :
2 ClO- + 4 H+ + 4 e- + 4 Fe2+ → Cl2 + 2 H2O + 4 Fe3+ + 4 e- - On simplifie les e- :
2 ClO- + 4 H+ + 4 Fe2+ → Cl2 + 2 H2O + 4 Fe3+
Deuxième exemple : un alcootest chimique (ou éthylotest chimique) est un dispositif permettant d'estimer le taux d'alcoolémie d'une personne. La personne souffle dans un petit tube contenant de la poudre de dichromate de potassium. Si l'haleine de la personne contient de l'alcool (éthanol), alors il se produit une réaction d'oxydo-réduction entre les ions dichromate (Cr2O72- de couleur jaune orangé) et l'éthanol (C2H6O) pour former des ions chrome III (Cr3+ de couleur verte) et de l'acide éthanoïque (C2H4O2).
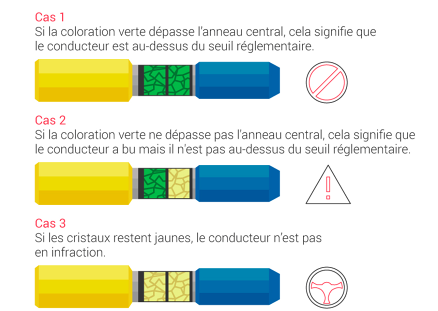 (Source : https://www.digischool.fr/cours/l-alcool-2)
(Source : https://www.digischool.fr/cours/l-alcool-2)
Les deux couples rédox mis en jeu sont : Cr2O72-/Cr3+ et C2H4O2/C2H6O
On applique alors la méthode précédente :
- Les réactifs sont les ions dichromate et l'éthanol. On écrit et on équilibre donc les deux demi-équations électroniques dans le bon sens, avec le réactif à gauche :
Cr2O72- + 14 H+ + 6 e- = 2 Cr3+ + 7 H2O
C2H6O + H2O = C2H4O2 + 4 H+ + 4 e- - On remarque que le nombre d'électrons mis en jeu dans chacune de ces deux demi-équations électroniques n'est pas le même : il y en a 6 dans la première, et 4 dans la deuxième. On va donc multiplier la première par 2 et la deuxième par 3 (car 6 × 2 = 4 × 3 = 12) :
2 Cr2O72- + 28 H+ + 12 e- = 4 Cr3+ + 14 H2O
3 C2H6O + 3 H2O = 3 C2H4O2 + 12 H+ + 12 e- - On additionne les deux demi-équations électroniques membre à membre :
2 Cr2O72- + 28 H+ + 12 e- + 3 C2H6O + 3 H2O → 4 Cr3+ + 14 H2O + 3 C2H4O2 + 12 H+ + 12 e- - On simplifie les ions H+, les molécules d'eau H2O ainsi que les e- :
2 Cr2O72- + 16 H+ + 3 C2H6O → 4 Cr3+ + 11 H2O + 3 C2H4O2
On retrouve bien l'équation donnée dans l'article suivant.