Quelques rappels
1./ Transformation chimique :
Lors d’une transformation chimique, des composés chimiques, appelés réactifs, réagissent entre eux et disparaissent, alors que de nouveaux composés, appelés produits, qui n’étaient pas présents au départ, apparaissent. Lors d’une transformation chimique, les composés chimiques présents à l’état initial (réactifs) ne sont pas les mêmes que ceux présents à l’état final (produits). Le changement de composition peut être visible à l’oeil nu : changement de couleur, dégagement gazeux, formation d’un précipité… Lorsque le changement n’est pas visible, on peut mettre en évidence la présence des produits en utilisant des tests.
Exemple vu au collège : lorsqu’on fait brûler du butane dans du dioxygène, il y a formation de dioxyde de carbone et de vapeur d’eau. La présence de dioxyde de carbone peut être prouvée grâce au test à l’eau de chaux ; la présence de vapeur d’eau peut être prouvée grâce au test au sulfate de cuivre anhydre.
2./ Modélisation d’une transformation chimique : réaction chimique :
La réaction chimique est un modèle simplifiée pour rendre compte des observations macroscopiques correspondant à la transformation chimique. Le bilan de la réaction chimique indique que les réactifs se transforment en produits. Les espèces chimiques se trouvant à gauche de la flèche sont les réactifs ; ceux se trouvant à droite de la flèche sont les produits.
Pour l’exemple précédent, le bilan serait : butane + dioxygène ➔ dioxyde de carbone + eau
3./ Ecriture symbolique d’une réaction chimique : l’équation chimique (ou équation-bilan) :
L’équation chimique est une traduction en langage chimique du bilan de la réaction chimique.
Pour l’exemple précédent, l’équation chimique serait : 2 C4H10 + 13 O2 ➔ 8 CO2 + 10 H2O
Les coefficients se trouvant devant les formules des différentes espèces chimiques, réactifs et produits, sont appelés coefficients stœchiométriques. Déterminer la valeur correcte de ces coefficients, c’est équilibrer, ou ajuster, l’équation chimique. Nous (re)verrons au prochain paragraphe la méthode d’équilibrage des équations chimiques.
4./ Notion d’espèce chimique spectatrice :
Une espèce chimique spectatrice est une espèce qui ne participe pas à une réaction chimique. Elle est présente avant et après la réaction, en quantité inchangée. On n’écrit généralement pas les espèces chimiques spectatrices dans les équations chimiques.
Exemples :
- L’air un est mélange de plusieurs gaz (environ 20% de dioxygène et 80% de diazote, si on néglige les autres gaz). Lorsqu’on fait brûler du carbone dans l’air (par exemple lors d’un barbecue), le carbone réagit avec le dioxygène présent dans l’air. Il y aura autant de diazote présent avant et après la réaction : le diazote ne participe pas à cette réaction. C’est donc une espèce chimique spectatrice. L’équation chimique de cette réaction est : C(s) + O2(g) ➔ CO2(g).
- Une solution d’acide chlorhydrique est une solution aqueuse qui contient des ions hydrogène (H+) et des ions chlorure (Cl–). Lorsqu’on plonge un morceau de fer (Fe) dans une solution d’acide chlorhydrique, celui-ci est attaqué et se dissout, et on observe un dégagement gazeux de dihydrogène (H2). Lors de cette réaction, les ions chlorure n’interviennent pas : il y en aura autant avant et après la réaction. Les ions chlorure sont une espèce chimique spectatrice. On peut aussi dire, dans ce cas-là, que les ions chlorure sont des ions spectateurs. On ne fera pas figurer ces ions dans l’équation chimique de la réaction est : Fe(s) + 2H+(aq) ➔ Fe2+(aq) + H2(g).
Comment écrire et équilibrer une équation chimique
1ère étape :
On recense d’abord les réactifs et les produits de la réaction. Si on prend l’exemple de la combustion du fer dans le dioxygène, les réactifs sont le fer et le dioxygène, et le produit est l’oxyde de fer. On écrit ensuite le bilan de la réaction chimique :
Fer + Dioxygène ➔ Oxyde de fer
2ème étape :
On remplace le nom des réactifs et des produits par leur symbole ou leur formule chimique. Dans notre exemple : Fer = Fe, Dioxygène = O2, Oxyde de fer = Fe3O4.
Fe + O2 ➔ Fe3O4
3ème étape :
On compte les différents atomes à gauche et à droite de la flèche. Si le nombre n’est pas le même, l’équation n’est pas équilibrée. On passe alors à l’étape suivante. Dans notre exemple :
A gauche : 1 atome de fer et 2 atomes d'oxygène
A droite : 3 atomes de fer et 4 atomes d'oxygène
4ème étape :
On équilibre l’équation de façon à avoir le même nombre d’atomes de chaque type à gauche et à droite de la flèche. Pour cela, il faut suivre les règles suivantes :
- On équilibre chaque type d’atomes séparément. Dans le cas de la combustion d’un métal, il est conseillé de commencer par équilibrer les atomes de métal, puis les atomes d’oxygène.
- Il ne faut JAMAIS modifier les formules des réactifs et des produits.
- Pour changer le nombre d’atomes, la seule façon est d’écrire des nombres (appelés coefficients) devant les formules des réactifs et des produits. Ces coefficients multiplient le nombre d’atomes contenus dans les formules qu’ils précèdent.
- Les coefficients d’une équation ne peuvent pas être des nombres à virgule. Les seuls coefficients valides sont des nombres entiers.
Pour éclaircir ces règles, reprenons notre exemple :
Fe + O2 ➔ Fe3O4
Il ne faut en aucun cas modifier les formules encadrées. La seule chose possible est d’écrire un coefficient devant un ou plusieurs des réactifs ou produits. Comme il s’agit d’une combustion d’un métal, nous allons commencer par équilibrer les atomes du métal (ici, le fer). Il y a 1 atome de fer à gauche, et 3 atomes de fer à droite. Pour passer de 1 à 3, il faut multiplier par 3. Nous allons donc placer le coefficient 3 devant Fe.
3 Fe + O2 ➔ Fe3O4
Il y a alors 3 × 1 = 3 atomes de fer à gauche et 3 atomes de fer à droite. Il nous reste à équilibrer les atomes d’oxygène. Il y en a 2 à gauche et 4 à droite. Pour passer de 2 à 4, il faut multiplier par 2. Nous allons donc placer le coefficient 2 devant O2.
3 Fe + 2 O2 ➔ Fe3O4
5ème étape :
On vérifie le nombre de chaque type d’atomes pour être sûr que l’équation est bien équilibrée.
Quelques vidéos reprenant l'essentiel de la méthode :
1ère remarque : dans le cas des combustions des hydrocarbures, il est conseillé d’équilibrer les atomes dans l’ordre suivant : carbone, hydrogène, puis oxygène. Exemple dans le cas de la combustion du méthane.
CH4 + O2 ➔ CO2 + H2O
Carbone : il y a 1 atome de carbone à gauche et à droite de la flèche. Il n’y a donc rien à faire au niveau des atomes de carbone.
Hydrogène : il y a 4 atomes d’hydrogène à gauche et 2 à droite. Pour passer de 2 à 4, il faut multiplier par 2. Nous allons donc placer le coefficient 2 devant H2O.
CH4 + O2 ➔ CO2 + 2 H2O
Oxygène : il y a 2 atomes d’oxygène à gauche, et 4 atomes d’oxygène à droite (2 dans CO2 et 2 dans 2 H2O). Pour passer de 2 à 4, il faut multiplier par 2. Nous allons donc placer le coefficient 2 devant O2.
CH4 + 2 O2 ➔ CO2 + 2 H2O
2ème remarque : dans certains cas, un coefficient à virgule apparaît : que faire dans ces cas-là ? Prenons un exemple, la combustion du butane (C4H10).
C4H10 + O2 ➔ CO2 + H2O
Carbone : il y a 4 atomes de carbone à gauche et un à droite de la flèche. Pour passer de 1 à 4, il faut multiplier par 4. Nous allons donc placer le coefficient 4 devant CO2.
C4H10 + O2 ➔ 4 CO2 + H2O
Hydrogène : il y a 10 atomes d’hydrogène à gauche et 2 à droite. Pour passer de 2 à 10, il faut multiplier par 5. Nous allons donc placer le coefficient 5 devant H2O.
C4H10 + O2 ➔ 4 CO2 + 5 H2O
Oxygène : il y a 2 atomes d’oxygène à gauche, et 13 atomes d’oxygène à droite (8 dans 4 CO2 et 5 dans 5 H2O). Pour passer de 2 à 13, il faut multiplier par 6,5 qui n’est pas un nombre entier. On multiplie donc par 2 tous les coefficients déjà placés :
2 C4H10 + O2 ➔ 8 CO2 + 10 H2O
Puis on recommence l’équilibrage de l’oxygène : il y a 2 atomes d’oxygène à gauche, et 26 atomes d’oxygène à droite (16 dans 8 CO2 et 10 dans 10 H2O). Pour passer de 2 à 26, il faut multiplier par 13. Nous allons donc placer le coefficient 13 devant O2.
2 C4H10 + 13 O2 ➔ 8 CO2 + 10 H2O
3ème remarque : dans certaines équations chimiques, il y a des ions. Afin que l’équation soit parfaitement équilibrée, il faut non seulement que le nombre d’atomes de chaque type soit le même à gauche et à droite de la flèche, mais il faut aussi que la somme des charges électriques soit la même à gauche et à droite.
Exemple : réaction de l’acide chlorhydrique et de l’aluminium :
Al + H+ ➔ Al3+ + H2
Il y a 1 charge + à gauche et 3 charges + à droite. On multiplie donc à gauche par 3 :
Al + 3 H+ ➔ Al3+ + H2
On a 3 atomes d’hydrogène à gauche et 2 à droite. Comme on ne peut pas passer de 2 à 3 en multipliant par un nombre entier, on multiplie tous les coefficients par 2.
2 Al + 6 H+ ➔ 2 Al3+ + H2
On a 3 atomes d’hydrogène à gauche et 2 à droite. On multiplie donc par 3 les atomes d’hydrogène du côté droit :
2 Al + 6 H+ ➔ 2 Al3+ + 3 H2
Vous pouvez vous entraîner sur le site suivant :
https://phet.colorado.edu/sims/html/balancing-chemical-equations/latest/balancing-chemical-equations_fr.html
Notion de réactif limitant ; proportions stœchiométriques
Nous avons vu que lors d’une réaction chimique, les réactifs disparaissaient et les produits apparaissaient. La réaction chimique s’arrête lorsque l’un au moins des réactifs a totalement disparu. Il y a deux possibilités :
- L’un des réactifs est totalement consommé, mais il reste des autres réactifs. Le réactif qui a totalement disparu est appelé réactif limitant. Les autres réactifs sont appelés des réactifs en excès.
- Si tous les réactifs disparaissent en même temps, on dit qu’ils ont été introduits dans les proportions stœchiométriques.
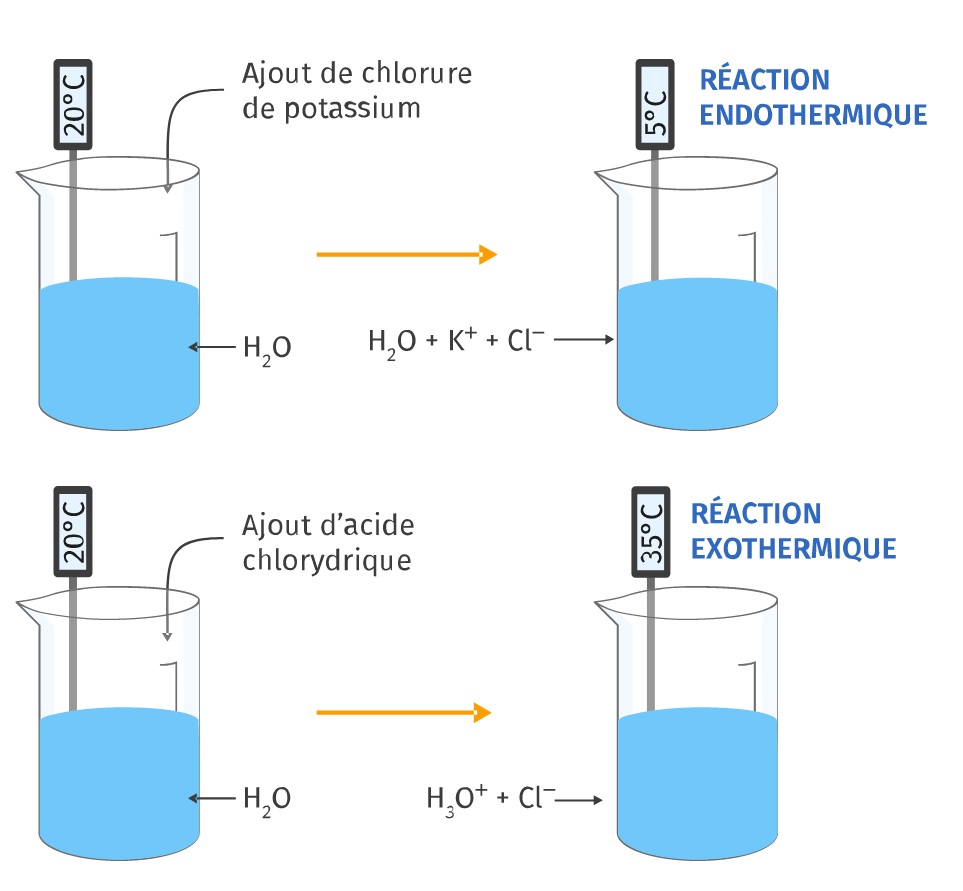
Transformations chimiques endothermiques et exothermiques
Certaines réactions chimiques se produisent en libérant de l’énergie thermique : la température du milieu s’élève pendant la réaction. On parle de réactions exothermiques. C’est par exemple le cas des combustions, ou de la réaction entre un acide et l’eau.
D’autres réactions chimiques vont absorber de l’énergie lorsqu’elles se produisent : la température du milieu diminue alors pendant la réaction. On parle de réactions endothermiques. C’est par exemple le cas de la dissolution du chlorure de potassium dans l’eau.
Une réaction qui n’est ni exothermique, ni endothermique est dite athermique. Il n’y a pas d’échange d’énergie avec le milieu extérieur lors de la réaction.