La lumière, une onde électromagnétique
Les ondes électromagnétiques correspondent à la propagation d’un champ électrique et d’un champ magnétique. Contrairement aux ondes mécaniques (comme les ondes sonores par exemple), les ondes électromagnétiques peuvent se déplacer en l’absence de milieu matériel, donc dans le vide. La lumière visible fait partie du spectre électromagnétique, comme les infrarouges (IR), les ultraviolets (UV), les rayons X, les ondes radio, etc… Ce qui rend les radiations visibles particulières, c’est le fait que l’œil humain puisse les détecter. Les ondes électromagnétiques se déplacent à la vitesse de la lumière.
Comme les ondes sonores, toute onde électromagnétique est caractérisée par sa fréquence \( f \) (ou ce qui revient au même, sa période \( T \)). On pourrait donc classer les différentes catégories d’ondes électromagnétiques en fonction de leur fréquence ; cependant les physiciens préfèrent utiliser une autre grandeur physique, la longueur d’onde \( \lambda \). La longueur d’onde s’exprime en m, et se calcule à partir de la période ou de la fréquence selon la formule suivante (qui n’est pas au programme) : \( \lambda=v\times T=\frac{v}{f} \)
Le calcul de la longueur d’onde dépendant aussi de \( v \), vitesse de propagation de l’onde électromagnétique dans le milieu matériel considéré, la longueur d’onde dépend donc de la nature du matériau traversé. Afin de classer les différentes catégories d’onde, on utilise la longueur d’onde dans le vide (\( v=c \)). La vitesse de la lumière dans l’air étant pratiquement égale à la vitesse de la lumière dans le vide, la longueur d’onde dans l’air est pratiquement égale à la longueur d’onde dans le vide.
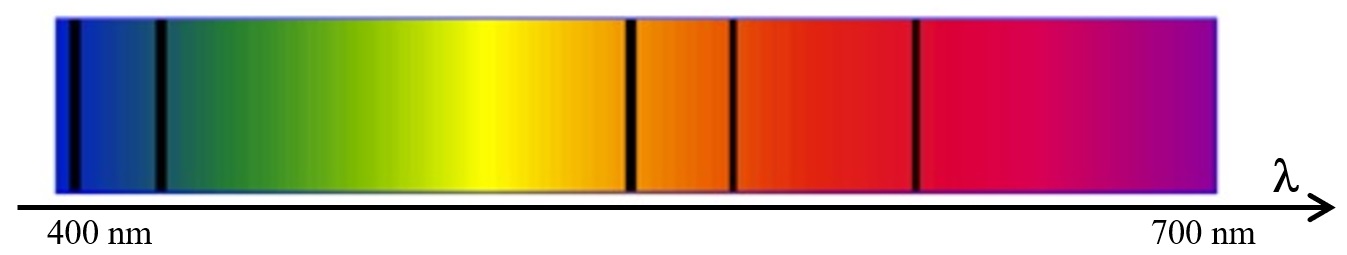
La lumière visible (ou spectre visible) est composée des ondes électromagnétiques dont la longueur d’onde (dans le vide) est comprise entre 400 nm et 700 nm environ (Rappel : 1 nm = 1 nanomètre = 1 × 10–9 m). En dessous de 400 nm se trouvent les rayonnements UV. Au-dessus de 700 nm, les rayonnements IR. A chaque longueur d’onde correspond une couleur particulière. Vers 400 nm, la lumière semblera violette, alors que vers 700 nm, elle semblera rouge. Il faut noter que la couleur de la lumière n’est pas une propriété physique réelle, c’est uniquement une interprétation faite par le cerveau de l’observateur. La seule grandeur physique réelle est la longueur d’onde.
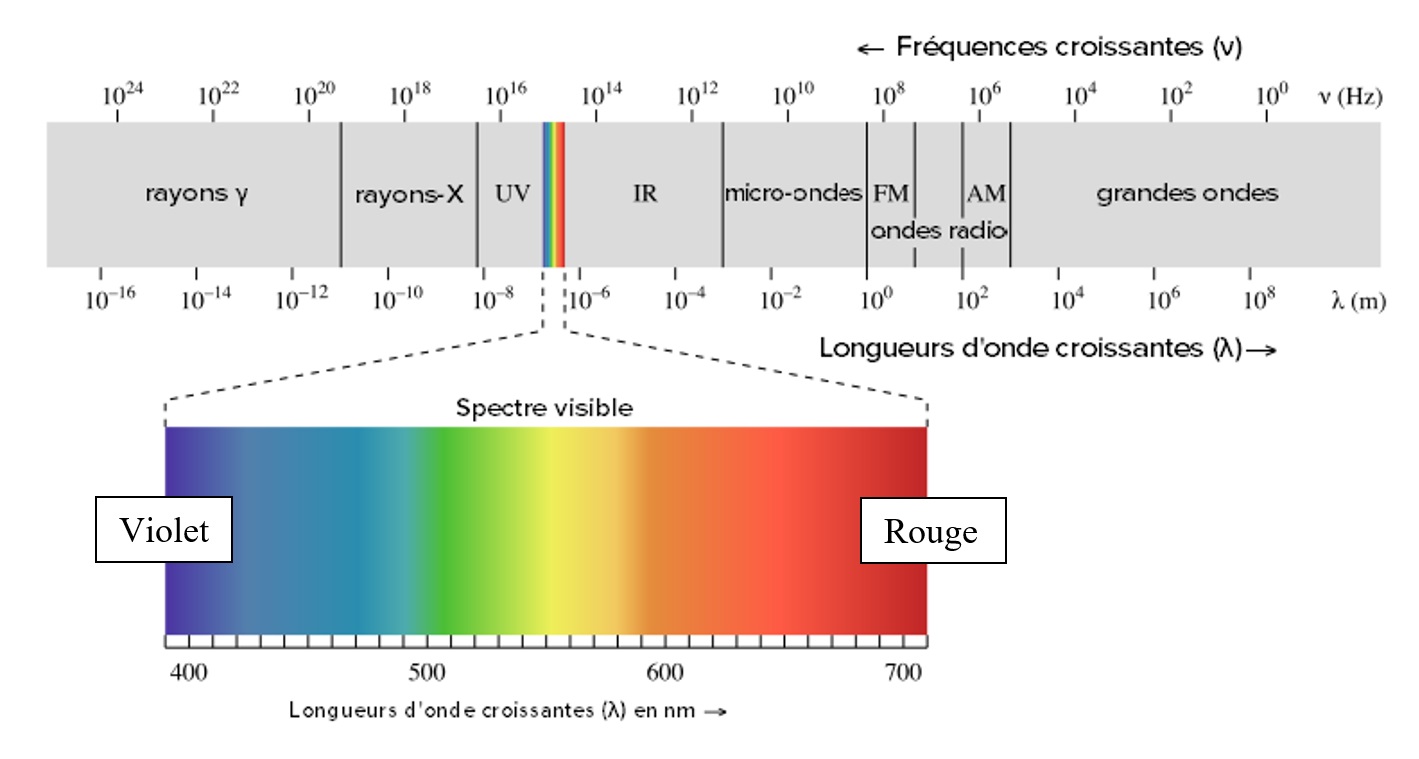
Pour étudier le spectre électromagnétique : http://physique.ostralo.net/oem_frise/.
On remarque que certaines couleurs ne sont pas présentes dans le spectre visible : on ne trouve pas, par exemple, le rose, le marron, le gris ou le blanc. Les couleurs présentes dans le spectre visible s’appellent des couleurs spectrales. Le mélange d’une ou plusieurs couleurs spectrales peut créer de nouvelles couleurs. Si on mélange toutes les longueurs d’onde comprises entre 400 et 700 nm, on obtient de la lumière blanche. Pour comprendre un peu mieux le phénomène :
Dispersion de la lumière
Certains milieux transparents sont dispersifs : leur indice de réfraction dépend de la longueur d’onde du rayon lumineux qui les traverse. Or la lumière blanche (par exemple la lumière du Soleil, ou d’une lampe) est la superposition de lumières colorées dont la longueur d’onde va de 400 nm (violet) à 700 nm environ (rouge). Chacune de ces lumières colorées sera donc déviée différemment. On peut donc séparer les différentes couleurs présentes dans la lumière blanche à l’aide d’un prisme : c’est ce qu’on appelle la dispersion de la lumière.
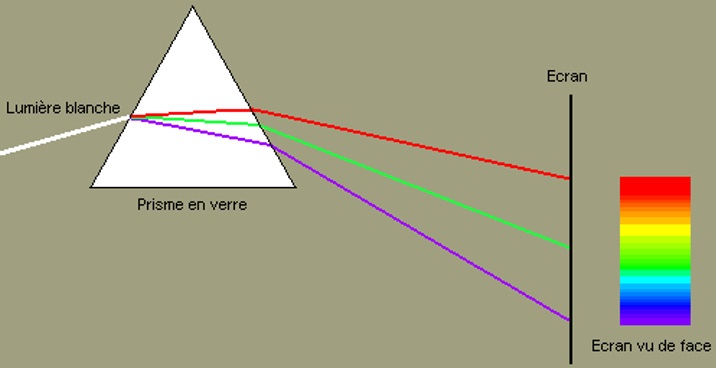
Lors de la traversée du prisme par la lumière blanche, ce sont les rayons violets qui sont le plus déviés, et les rayons rouges qui sont le moins déviés. Si on place un écran derrière le prisme, on obtient le spectre de la lumière blanche.
Cette expérience a été réalisée en 1966 par le physicien anglais Issac Newton :

Spectres d’émission continus, d’origine thermique
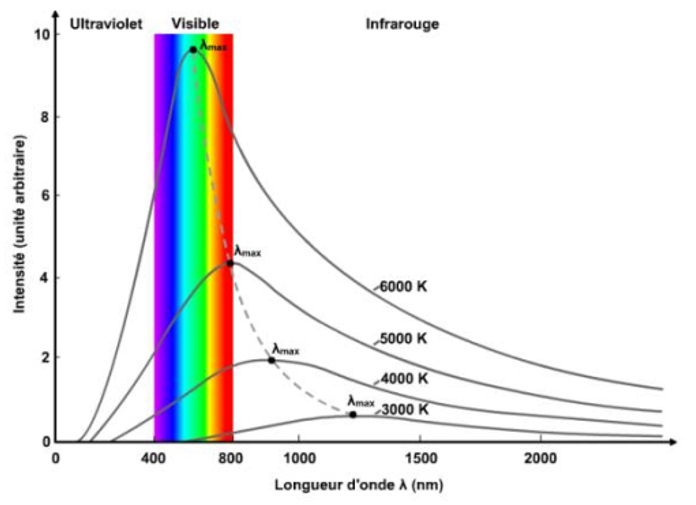
Un corps dense (solide, liquide ou gaz sous haute pression) porté à haute température émet de la lumière. Le spectre de la lumière émise est un spectre continu. Plus la température de la source lumineuse est importante, plus le maximum d’émission se déplace vers les petites longueurs d’onde. Un morceau de métal chauffé va d’abord émettre des IR, puis va devenir rouge sombre, orangé puis blanc : au fur et à mesure que la température augmente, le spectre va s’enrichir progressivement vers le violet. A partir d’une certaine température (environ 2000°C), le spectre de la lumière émise contient toutes les radiations visibles, mais avec des intensités différentes. La couleur dominante d’un spectre continu (celle qui est la plus lumineuse) donne une indication de la température de la source.
Spectres de raies
Le spectre de la lumière émise par un gaz sous faible pression et à haute température est un spectre de raies. Chaque atome (et chaque ion) possède un spectre de raies bien déterminé, qui correspond à une carte d’identité de l’espèce chimique étudiée. Voici par exemple le spectre d’émission de l’atome de mercure :

Un atome (ou un ion) peut aussi absorber les longueurs d’onde qu’il est capable d’émettre. Dans certaines conditions, on peut donc obtenir son spectre d’absorption, qui sera le complémentaire de son spectre d’émission. Exemple pour le mercure :
Vous pouvez illustrer le phénomène avec l'animation suivante : https://physique.ostralo.net/spectre_em_abs/