Définitions et vocabulaire
Lors d’une transformation chimique, les réactifs disparaissent, et des produits apparaissent. Le modèle descriptif de la transformation chimique est la réaction chimique. L’écriture symbolique de la réaction chimique est l’équation chimique.
Une équation chimique se présente sous la forme :
a A + b B → c C + d D
où A et B sont les réactifs, C et D sont les produits. Les nombres a, b, c et d sont les coefficients stœchiométriques.
Tableau descriptif de l’évolution d’un système lors d’une transformation chimique
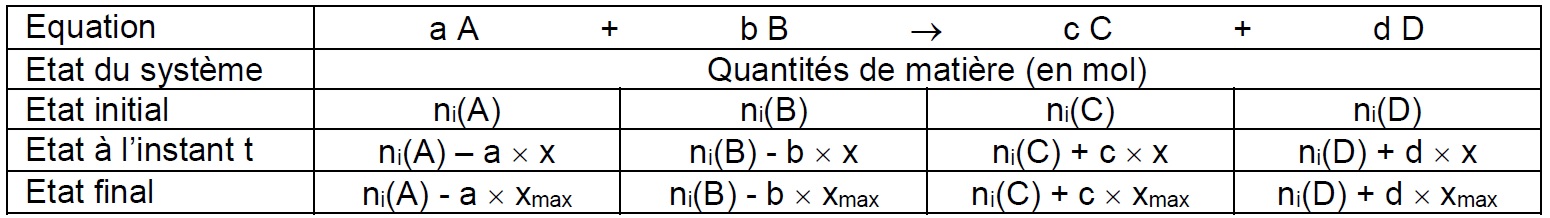
Le nombre x est l’avancement de la réaction. Il s’exprime en mol. Le nombre xmax est l’avancement maximal, c’est-à-dire l’avancement de la réaction lorsque le système a fini d’évoluer. On a alors atteint l’état final. Cela se produit lorsque la quantité de matière d’au moins un des réactifs devient nulle. Ce réactif est appelé le réactif limitant. Le ou les réactifs encore présents à l’état final sont appelés réactifs en excès. Dans notre cas, xmax est atteint lorsque ni(A) - a × xmax = 0 ou ni(B) - b × xmax = 0.
Cas particulier du mélange stœchiométrique : lorsque les réactifs sont introduits dans les proportions stœchiométriques de la réaction, seuls les produits sont présents à l’état final. Il n’y a pas de réactif limitant.
Lorsque l’état final est atteint, le tableau descriptif permet de faire un bilan de matière : c’est l’inventaire quantitatif des espèces présentes à l’état final.
Quelques exemples
1./ Combustion de l’éthanol :
Soit l’équation chimique suivante, correspondant à la réaction de combustion complète de l’éthanol :
C2H6O + 3 O2 → 2 CO2 + 3 H2O
On va prendre l’exemple d’un mélange composé de 3 moles d’éthanol et de 6 moles de dioxygène. On considère qu’il n’y a ni dioxyde de carbone, ni eau à l’instant initial.

L’avancement maximal est atteint lorsqu’il n’y a plus d’éthanol ou lorsqu’il n’y a plus de dioxygène.
Supposons que ce soit l’éthanol le réactif limitant : on a alors : 3 – xmax = 0, soit xmax = 3 mol. La quantité de matière de dioxygène est alors égale à 6 – 3 × 3 = – 3 mol, ce qui est absurde.
Le réactif limitant est donc le dioxygène, et 6 – 3xmax = 0, donc : xmax = 2 mol.
Bilan de matière : à l’état final, le système est composé d’une mole d’éthanol, de 4 moles de dioxyde de carbone et de 6 moles d’eau.
Représentation graphique de l’évolution du système : Pour mieux visualiser l’évolution du système, on peut représenter la quantité de matière des différents réactifs et produits en fonction de l’avancement de la réaction.
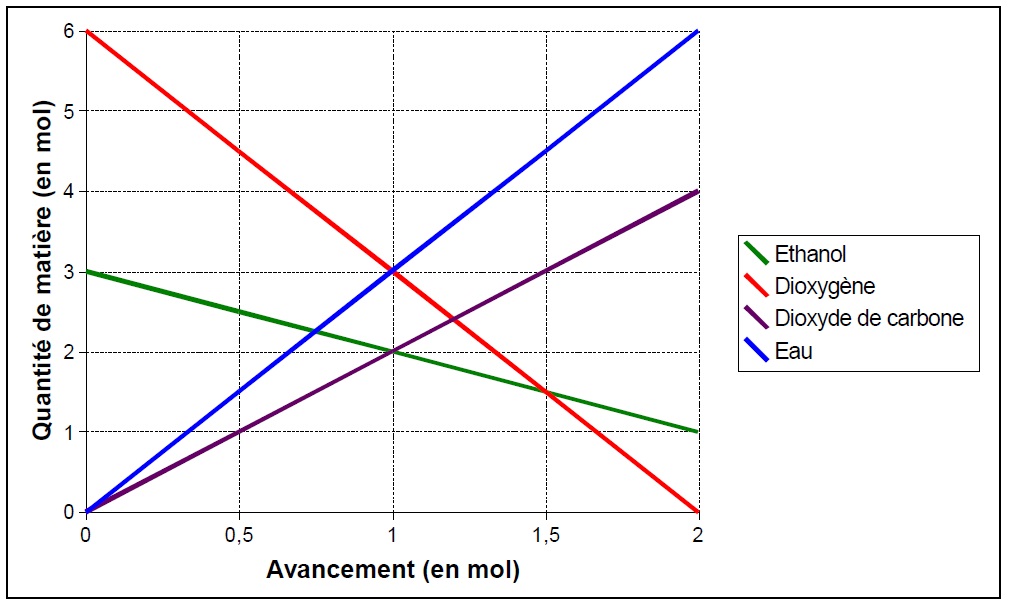
Mélange stœchiométrique : dans quelles conditions le mélange est-il stœchiométrique ? Soit n(C2H6O)i et n(O2)i les quantités de matière initiales d’éthanol et de dioxygène.
Si le mélange est stœchiométrique, on a : n(C2H6O)i – xmax = n(O2)i – 3xmax = 0.
On a alors, dans ces conditions : n(C2H6O)i = xmax et n(O2)i = 3xmax, soit n(C2H6O)i / n(O2)i = 1 / 3.
Pour que le mélange soit stoechiométrique, il faut donc que le rapport des quantités de matière de réactifs à l’état initial soit égal au rapport des coefficients stoechiométriques des réactifs dans l’équation chimique.
Le bilan de matière sera alors : n(C2H6O)final = n(O2)final = 0, n(CO2)final = 2xmax et n(H2O)final=3xmax. Si on utilise par exemple 2 moles d’éthanol et 6 moles de dioxygène, il y aura après réaction 4 moles de dioxyde de carbone et 6 moles d’eau :
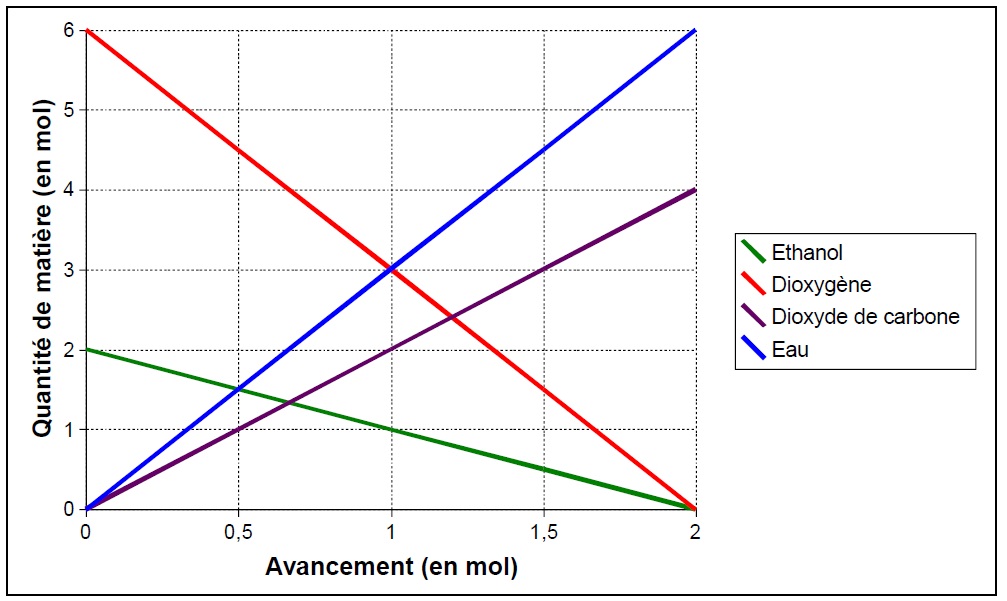
Application : On veut faire brûler 2,3 grammes d’éthanol. Quel est le volume minimum de dioxygène nécessaire ? Après refroidissement, quel est le volume de dioxyde de carbone que l’on obtient ? Quelle est la masse d’eau récupérée ? On considère que dans les conditions de l’expérience, le volume molaire du gaz parfait est Vm = 24 L·mol-1.
Solutions :
Le nombre de moles d’éthanol est : n(C2H6O)i = m / M = 2,3 / 46 = 0,05 moles. Il faut donc 0,15 moles de dioxygène pour réaliser cette combustion, soit un volume de : V = 0,15 × Vm = 3,6 litres. On obtient 0,10 moles de dioxyde de carbone, soit un volume de 2,4 litres (après refroidissement), et 0,15 moles d’eau, soit une masse de 2,7 grammes.
2./ Réaction de l’aluminium avec l’acide chlorhydrique :
Soit l’équation chimique suivante, correspondant à la réaction de l’attaque de l’aluminium par l’acide chlorhydrique :
2 Al + 6 (H+ + Cl-) → 2 (Al3+ + 3 Cl-) + 3 H2
L’équation simplifiée de cette réaction est :
2 Al + 6 H+ → 2 Al3+ + 3 H2
a./ Faire le tableau d’avancement dans le cas où les quantités de matière initiale sont respectivement de 2 moles d’aluminium et de 3 moles d’acide chlorhydrique :

b./ Quel est le réactif limitant ? Quel est le bilan de matière à l’instant final ?
Si on fait l’hypothèse que c’est l’aluminium le réactif limitant, on obtient xmax = 1 mol.
Si on considère que c’est l’acide chlorhydrique, on obtient xmax = 0,5 mol.
Le réactif limitant est donc l’acide chlorhydrique, et l’avancement final est donc xmax = 0,5 mol.
Le bilan de matière est donc : 1 mole d’aluminium, 1 mole d’ions aluminium (Al3+) et 1,5 moles de dihydrogène.
c./ Faire un diagramme montrant l’évolution des quantités de matière des différents réactifs et produits en fonction de l’avancement de la réaction :
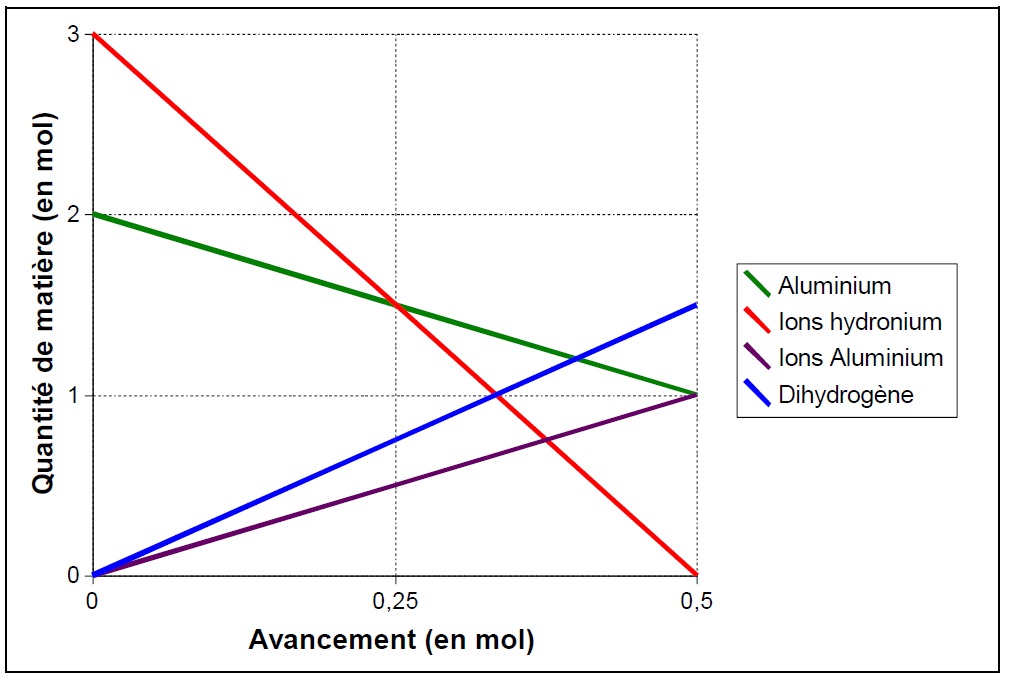
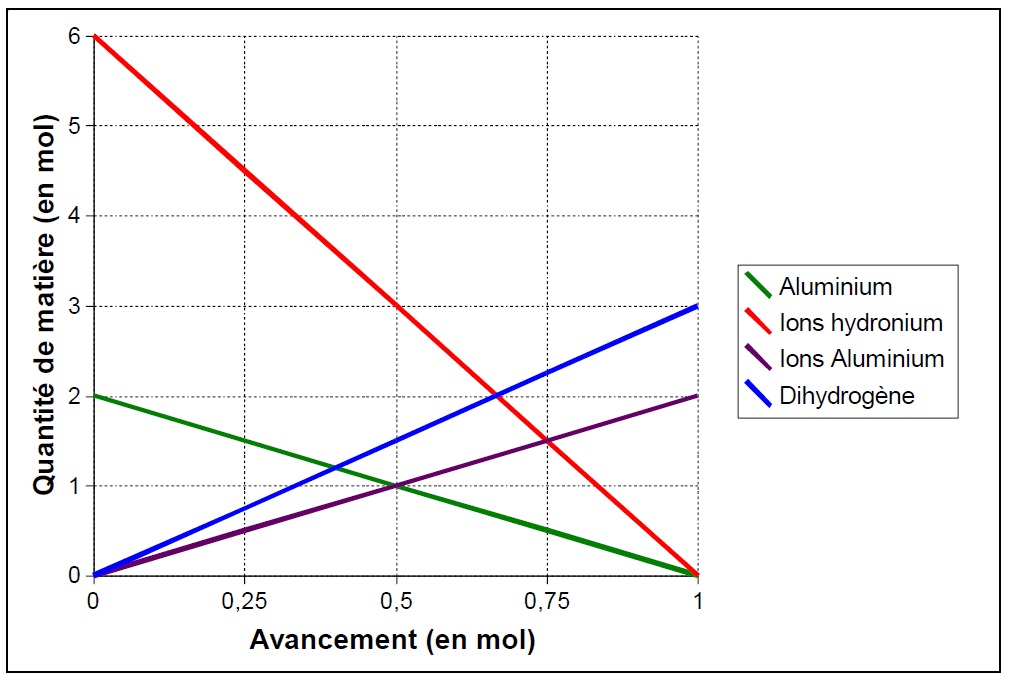
d./ On veut partir d’un mélange stœchiométrique comportant 2 moles d’aluminium. Combien faut-il de moles d’acide chlorhydrique ? Quel est alors le bilan de matière ? Refaire le diagramme correspondant à cette situation :
Les coefficients relatifs à Al et H+ dans l’équation chimique sont respectivement de 2 et de 6.
Pour être dans les proportions stœchiométriques, il faut que n(Al)i / n(H+)i = 2 / 6. Comme on a : n(Al)i = 2 mol, alors : n(H+)i = 6 mol.
L’avancement maximal est alors xmax = 1, et le bilan de matière nous donne 2 moles d’ions aluminium et 3 moles de dihydrogène.
Une petite animation pour visualiser la notion d'avancement sur le site Ostralo.