Doser (ou titrer) une solution consiste à déterminer la concentration d’une espèce chimique dans cette solution. Il existe de très nombreuses méthodes de dosage. Parmi toutes ces méthodes, nous allons nous intéresser à deux techniques de dosages colorimétriques : le dosage spectrophotométrique par étalonnage, et le titrage colorimétrique.
Dosage spectrophotométrique par étalonnage
Dans les dosages par étalonnage, on compare une grandeur physique de la solution à doser (par exemple, l’absorbance, la conductivité, la masse volumique, etc…) à la même grandeur physique mesurée pour des solutions étalons. Il s'agit de techniques de dosage non destructives, car ne modifiant pas la solution étudiée.
La spectrophotométrie est une technique d’analyse qui repose sur l’absorption de la lumière par les espèces chimiques colorées. Une solution est colorée si elle absorbe une partie des radiations de la lumière blanche, la couleur perçue résultant de la superposition des teintes des radiations non absorbées.
Un spectrophotomètre mesure l’absorbance \( A \) (grandeur sans unité) d’une solution diluée colorée contenue dans une cuve. Cette absorbance dépend de la longueur d'onde de la lumière incidente. En traçant l'absorbance d'une solution pour toutes les longueurs d'onde de la lumière visible, toutes choses étant égales par ailleurs, on peut tracer le spectre d'absorption de la substance chimique étudiée.
Voici par exemple le spectre d'absorption du permanganate de potassium en solution aqueuse :
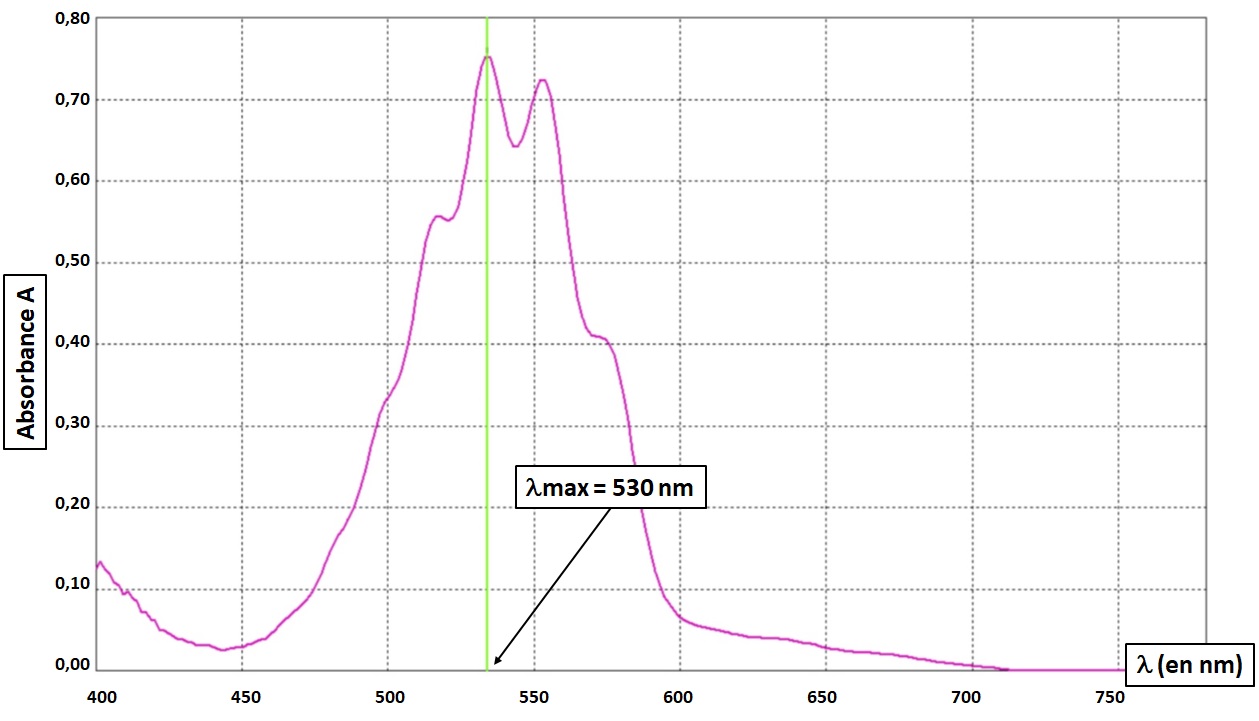
On remarque que le maximum d'absorption du permanganate de potassium se situe aux alentours de la longueur d'onde \( \lambda \) = 530 nm, ce qui correspond à la couleur verte. La couleur de la solution correspond à la couleur complémentaire, que l'on peut retrouver grâce au cercle chromatique :
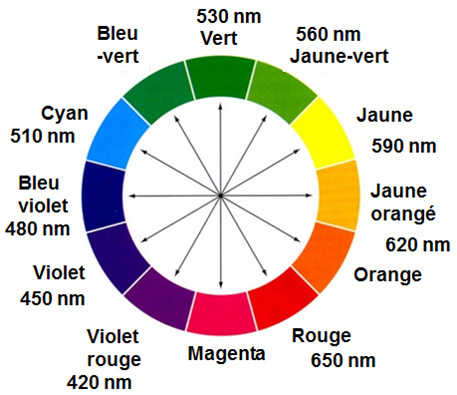
La solution aqueuse de permanganate de potassium a donc une teinte magenta.
Pour une longueur d'onde \( \lambda \) donnée, l'absorbance d'une solution est donnée par la relation de Beer-Lambert :
\( A=\epsilon(\lambda)\times l\times C \)
Avec : \( A \) l'absorbance de la solution (nombre sans unité), \( \epsilon(\lambda) \) le coefficient d'extinction molaire (en L·mol-1·cm-1) qui dépend de la longueur d'onde \( \lambda \), \( l \) la largeur de la cuve (en cm) et \( C \) la concentration molaire (en mol·L-1).
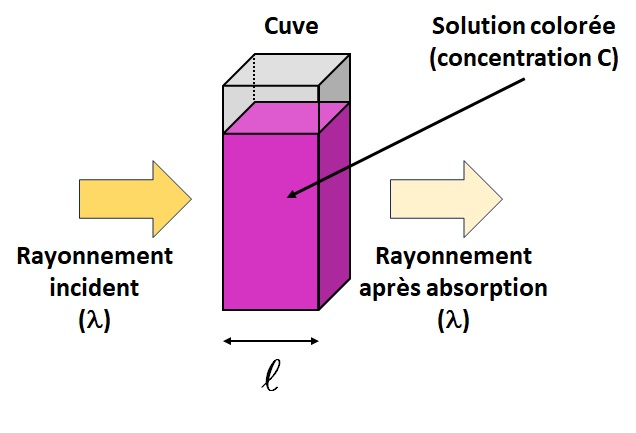
Si on pose : \( k=\epsilon(\lambda)\times l \) alors on peut écrire : \( A=k\times C \)
On peut donc dire que pour une longueur d'onde et une largeur de cuve donnée, l'absorption d'une solution est proportionnelle à la concentration molaire de l'espèce chimique colorée en solution. Cela permet de réaliser un dosage par étalonnage :
- Afin d’avoir une meilleure précision, on se place à la longueur d’onde qui correspond à un maximum d’absorbance de la substance. Si on utilise un appareil n’ayant qu’un nombre limité de longueurs d’onde (comme le colorimètre utilisé en T.P.), on se place à la longueur d’onde la plus proche d’un maximum d’absorbance. Dans notre exemple, avec le permanganate de potassium, on se placerait donc à \( \lambda \) = 530 nm.
- On réalise une échelle de teinte, c'est-à-dire des solutions ayant des concentrations connues, par dilution d'une solution mère plus concentrée. Voilà ce que ça donne dans le cas du permanganate de potassium :
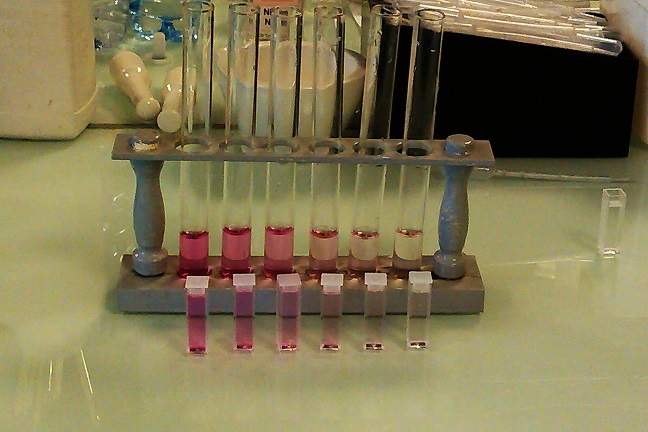
- On mesure l'absorbance de chacune de ces solutions, et on trace le graphique de l'absorbance en fonction de la concentration. On modélise ensuite les résultats expérimentaux par un modèle linéaire, du type : \( A=k\times C \). Voici le graphique obtenu avec les solutions de notre exemple, ainsi que le modèle linéaire correspondant :
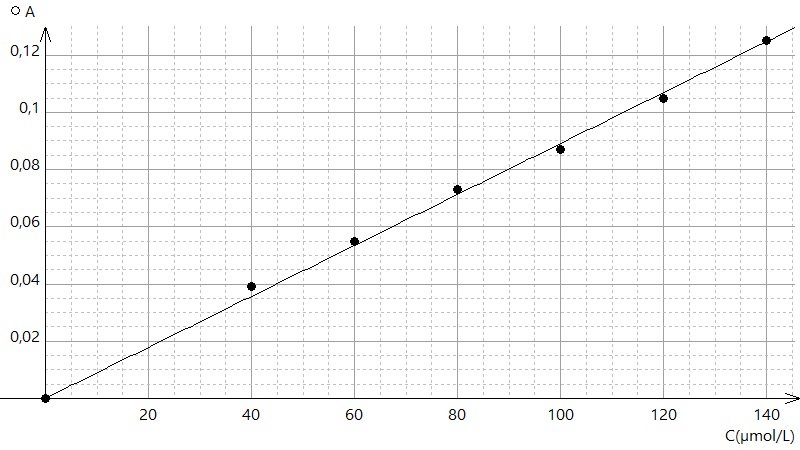
- Il suffit alors de mesurer l'absorbance d'une solution dont on ne connait pas la concentration, pour calculer cette dernière à l'aide du modèle.
- Attention, il est à noter que la relation de Beer-Lambert n'est plus correcte pour des solutions très concentrées. Il faudra donc assez souvent diluer la solution à doser avant de réaliser la manipulation.
Titrage direct colorimétrique
Réaliser un titrage direct, c’est faire réagir l’espèce chimique à titrer avec une quantité connue d’une espèce chimique titrante. La réaction chimique entre les deux espèces doit être rapide et totale : on parle de réaction quantitative. Contrairement au dosage spectrophotométrique, il s'agit là d'une technique de dosage destructive.
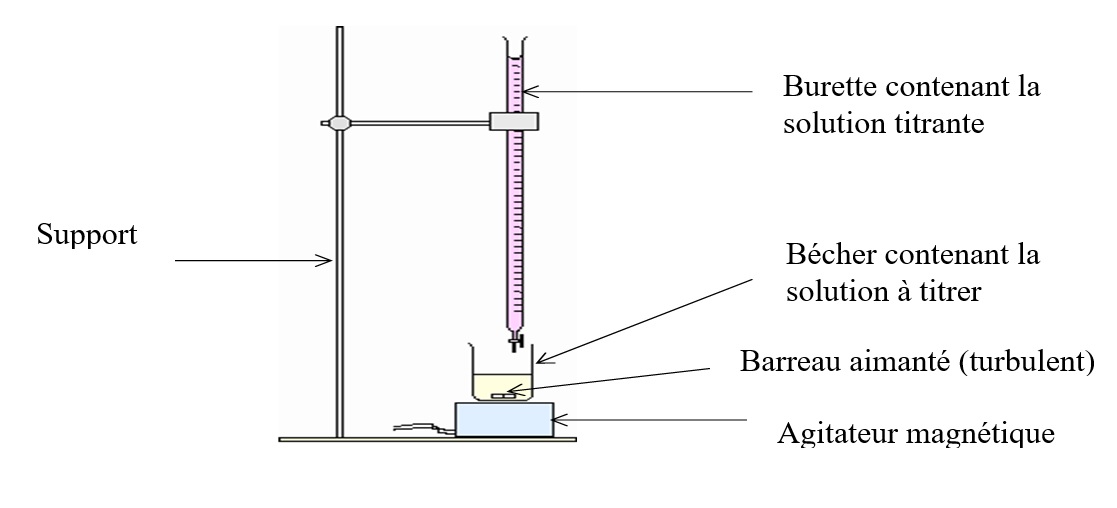
La réaction support d’un dosage est la réaction chimique entre l’espèce à titrer (notée A) et l’espèce titrante (notée B) :
a A + b B → c C + d D
(avec : a, b, c et d, les coefficients stœchiométriques de l’équation de la réaction support du titrage).
Equivalence d’un titrage :
L’équivalence d’un titrage correspond au moment où les réactifs sont introduits dans les proportions stœchiométriques. On change alors de réactif limitant. Avant l’équivalence, c’est l’espèce chimique titrante qui est le réactif limitant. Après l’équivalence, il s’agit de l’espèce chimique à titrer.
Dans le cadre d'un titrage colorimétrique, on sait que l'on a atteint l'équivalence car l'un au moins des réactifs ou des produits est coloré : il va donc y avoir un changement de couleur du milieu réactionnel quand on atteint le point d'équivalence. On peut aussi utiliser un indicateur coloré, qui est une espèce chimique qui va changer de couleur au moment de l'équivalence.
Soit \( n_{0}(A) \) la quantité de matière de l’espèce à titrer A présente dans le bécher à l’instant initial : \( n_{0}(A)=C_{A}\times V_{A} \).
\( C_{A} \) est la concentration de la solution à titrer (qui est donc inconnue avant le titrage !) et \( V_{A} \) est le volume de solution à titrer introduite dans le bécher.
Soit \( n_{0}(B) \) la quantité de matière de l’espèce titrante B introduite à l’équivalence : \( n_{0}(B)=C_{B}\times V_{éq} \).
\( C_{B} \) est la concentration de la solution titrante (qui est donc connue) et \( V_{éq} \) est le volume de solution titrante versée au moment de l'équivalence.
On construit le tableau d’avancement correspondant :

A l’équivalence, on est dans les proportions stœchiométriques, et les deux réactifs sont donc entièrement et simultanément consommés.
On a alors : \( n_{0}(A)-a\times x_{max}=0 \) et : \( n_{0}(B)-b\times x_{max}=0 \)
Soit : \( x_{max}=\frac{n_{0}(A)}{a} \) et : \( x_{max}=\frac{n_{0}(B)}{b} \)
On a donc: \( \frac{n_{0}(A)}{a}=\frac{n_{0}(B)}{b} \)
Or on sait que : \( n_{0}(A)=C_{A}\times V_{A} \)
et que : \( n_{0}(B)=C_{B}\times V_{éq} \)
On peut donc écrire que :
\( \frac{C_{A}\times V_{A}}{a}=\frac{C_{B}\times V_{éq}}{b} \)
De cette expression, on peut obtenir la valeur de la concentration de la solution à titrer :
\( C_{A}=\frac{a\times C_{B}\times V_{éq}}{b\times V_{A}} \)
Prenons par exemple la réaction du titrage de la vidéo précédente : la solution à titrer A est une solution de diiode (I2), et la solution titrante B est une solution de thiosulfate de sodium (2 Na+ + S2O32-).
La réaction support du titrage est :
I2 + 2 S2O32- → 2 I- + S4O62-
On a donc : a = 1 et b = 2 et on peut écrire que : \( \frac{C_{I_{2}}\times V_{I_{2}}}{1}=\frac{C_{S_{2}O_{3}^{2-}}\times V_{éq}}{2} \)
Et on peut déterminer la concentration en diiode avec la relation suivante : \( C_{I_{2}}=\frac{1\times C_{S_{2}O_{3}^{2-}}\times V_{éq}}{2\times V_{I_{2}}} \)