Quelques rappels
1./ Le noyau atomique :
L’atome est composé d’un noyau central, entouré d’un nuage électronique. Le noyau se trouve au centre de l’atome. Il est formé de particules appelées nucléons. Il y a deux types de nucléons : les protons, chargés positivement et les neutrons, électriquement neutres. Un noyau atomique particulier est désigné par une notation symbolique qui indique la composition et la nature de ce noyau :

2./ Isotopes :
Tous les atomes d’un même élément ont, par définition, le même nombre de protons dans leur noyau. Par contre, ils peuvent avoir un nombre de neutrons différents.

Transformations nucléaires
1./ Lois de Soddy :
Les lois de Soddy disent que lors d’une transformation nucléaire, il y a conservation de la charge électrique et conservation du nombre de masse.
Les deux particules constituant le noyau sont le proton et le neutron. Pour le proton, chargé positivement, on a : Z = 1 (une charge positive) et A = 1 (un nucléon). La notation symbolique du proton est donc : \( \mathrm{}_{1}^{1}p \). Pour le neutron, neutre électriquement, on a : Z = 0 (charge électrique nulle) et A = 1 (un nucléon). La notation symbolique du neutron est donc : \( \mathrm{}_{0}^{1}n \).
Dans certaines transformations nucléaires, des particules autres que les nucléons (protons et neutrons) peuvent parfois intervenir, comme l’électron (e<sup>–</sup>) ou le positon (e<sup>+</sup>), qui est une particule presqu’identique à l’électron mais qui possède une charge positive (le positon est l’antiparticule de l’électron ; on l’appelle aussi positron ou antiélectron). La notation symbolique de l’électron est : \( \mathrm{}_{-1}^{0}e^{-} \) et celle du positon est : \( \mathrm{}_{+1}^{0}e^{+} \).
Contrairement aux réactions chimiques, il n’y a pas forcément les mêmes éléments chimiques avant et après une réaction nucléaire.
2./ Radioactivité :
Certains noyaux sont instables : ils se transforment spontanément en d’autres noyaux, plus stables en émettant une ou plusieurs particules, selon une équation de réaction du type :
\( \mathrm{}_{Z}^{A}X\to \mathrm{}_{Z'}^{A'}Y+\mathrm{}_{Z''}^{A''}particule \)
Le noyau de départ \( \mathrm{}_{Z}^{A}X \) est appelé noyau père ; le noyau d’arrivée \( \mathrm{}_{Z'}^{A'}Y \) est appelé noyau fils. Les règles de Sody permettent d’écrire que : \( A=A'+A'' \) et que : \( Z=Z'+Z'' \). Cette réaction est appelée désintégration radioactive. Selon la nature de la particule émise, on observe plusieurs types de désintégrations.
a./ La désintégration α (alpha) :
La particule émise est un noyau d’hélium \( \mathrm{}_{2}^{4}He \) (un noyau composé de 2 protons et de 2 neutrons), aussi appelé particule α. La réaction correspondante est :
\( \mathrm{}_{Z}^{A}X\to \mathrm{}_{Z-2}^{A-4}Y+\mathrm{}_{2}^{4}He \)
Exemple : \( \mathrm{}_{88}^{226}Ra\to \mathrm{}_{86}^{222}Rn+\mathrm{}_{2}^{4}He \)
b./ La désintégration β- (béta moins) :
La particule émise est un électron \( \mathrm{}_{-1}^{0}e^{-} \). La réaction correspondante est :
\( \mathrm{}_{Z}^{A}X\to \mathrm{}_{Z+1}^{A}Y+\mathrm{}_{-1}^{0}e^{-} \)
Exemple : \( \mathrm{}_{82}^{209}Pb\to \mathrm{}_{83}^{209}Bi+\mathrm{}_{-1}^{0}e^{-} \)
c./ La désintégration β+ (béta plus) :
La particule émise est un positon \( \mathrm{}_{+1}^{0}e^{+} \). La réaction correspondante est :
\( \mathrm{}_{Z}^{A}X\to \mathrm{}_{Z-1}^{A}Y+\mathrm{}_{1}^{0}e^{+} \)
Exemple : \( \mathrm{}_{82}^{205}Pb\to \mathrm{}_{81}^{205}Tl+\mathrm{}_{1}^{0}e^{+} \)
3./ Fission nucléaire :
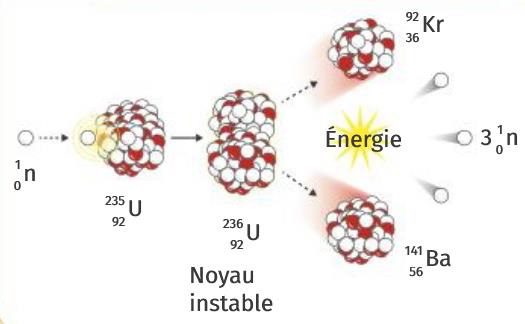
Dans une réaction de fission nucléaire, un noyau lourd dit fissile se casse en deux noyaux plus légers et quelques neutrons. Si la réaction se fait sans aide extérieure, on parle de fission nucléaire spontanée. Si la réaction se fait à l’aide du choc avec un neutron, on parle de fission nucléaire provoquée. C’est ce type de réaction qui est utilisé pour fabriquer de l’électricité dans les centrales nucléaires.
Exemple : \( \mathrm{}_{92}^{235}U+\mathrm{}_{0}^{1}n\to \mathrm{}_{36}^{92}Kr+\mathrm{}_{56}^{141}Ba+3\mathrm{}_{0}^{1}n \)
4./ Fusion nucléaire :
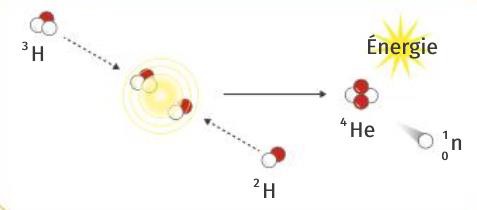
Dans une réaction de fusion nucléaire, deux noyaux légers s’assemblent entre eux pour former un noyau plus lourd, avec émission éventuelle d’un ou de plusieurs neutrons. C’est ce type de réaction qui se déroule au cœur des étoiles.
Exemple : \( \mathrm{}_{1}^{2}H+\mathrm{}_{1}^{3}H\to \mathrm{}_{2}^{4}He+\mathrm{}_{0}^{1}n \)
Aspects énergétiques
1./ Radioactivité :
Lors des désintégrations radioactives, de l’énergie est libérée sous forme de rayonnement. Ce phénomène peut être utilisé en médecine dans le cadre de la radiothérapie.
2./ Réaction de fission nucléaire :
Les réactions de fission nucléaire libèrent une très grande quantité d’énergie qui peut être convertie en énergie électrique dans les réacteurs des centrales nucléaires (et dans les bombes nucléaires, ou bombes A).
3./ Réaction de fusion nucléaire :
Les réactions de fusion nucléaire sont encore plus énergétiques que les réactions de fission. Ce sont elles qui expliquent le rayonnement des étoiles. Ce type de réaction est aussi utilisé dans les bombes thermonucléaires, ou bombes H. On ne sait pas encore maîtriser la fusion, mais plusieurs expériences sont en cours comme ITER, à Cadarache, ou le Laser Mégajoule, non loin de Bordeaux.
Vidéo "Monsieur Prudent découvre la radioactivité" :