Quelques définitions
- Entité chimique : il s’agit d’une molécule, d’un atome ou d’un ion.
- Espèce chimique : c’est un ensemble d’entités chimiques identiques. Exemple : sucre, eau, fer, soufre, chlorure de sodium…
- Corps pur : un corps pur est composé d’une seule espèce chimique.
- Corps pur simple : un seul type d’atomes. Exemple : le carbone C, l’or Au, le dioxygène O2, le diazote N2, l’ozone O3, …
- Corps pur composé : plusieurs types d’atomes. Exemple : l’eau H2O, l’éthanol C2H6O, le glucose C6H12O6, la nitroglycérine C3H5N3O9, …
- Mélange : un mélange est composé de plusieurs espèces chimiques différentes.
- Mélange homogène : il y a une seule phase : on ne peut pas distinguer les différents composants à l’œil nu. Exemple : eau salée, eau sucrée, eau + sirop, …
- Mélange hétérogène : il y a plusieurs phases : on peut distinguer les différents composants à l’œil nu. Exemple : eau + huile, eau + sable, …
- Miscibles : deux liquides sont miscibles lorsqu’ils forment ensemble un mélange homogène (exemple : eau + éthanol). Dans le cas contraire, on dit que les liquides ne sont pas miscibles (exemple : eau + huile).
Propriétés physiques des espèces chimiques
1./ Masse volumique :
La masse volumique d'un matériau se calcule de la façon suivante :
\( \rho=\frac{m}{V} \)
Avec : \( m \) la masse de l'échantillon (en g, ou en kg), \( V \) le volume de l'échantillon (en cm3 ou en L) et \( \rho \) la masse volumique (en g·cm-3 ou en kg·L-1).
La masse volumique est parfois notée \( \mu \).
Note : la densité du matériau est donnée par la relation suivante :
\( d=\frac{\rho}{\rho_{eau}} \)
Avec : \( \rho \) la masse volumique du matériau et \( \rho_{eau} \) la masse volumique de l'eau. Ces deux masses volumiques doivent être exprimées dans la même unité. La densité \( d \) est un nombre sans unité.
Exemples de masses volumiques :
- \( \rho_{eau} \) = 1,00 g·cm-3 = 1,00 kg·L-1 (à 20°C)
- \( \rho_{glace} \) = 0,92 g·cm-3 = 0,92 kg·L-1 (à 0°C)
- \( \rho_{eau} \) = 0,789 g·cm-3 = 0,789 kg·L-1 (à 0°C)
2./ Changement d'état :
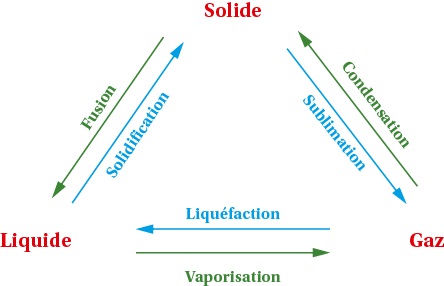
Pour un corps pur, un changement d’état se produit à une température donnée, qui dépend de l’espèce chimique considérée. Pour un mélange, la température varie lors d’un changement d’état.
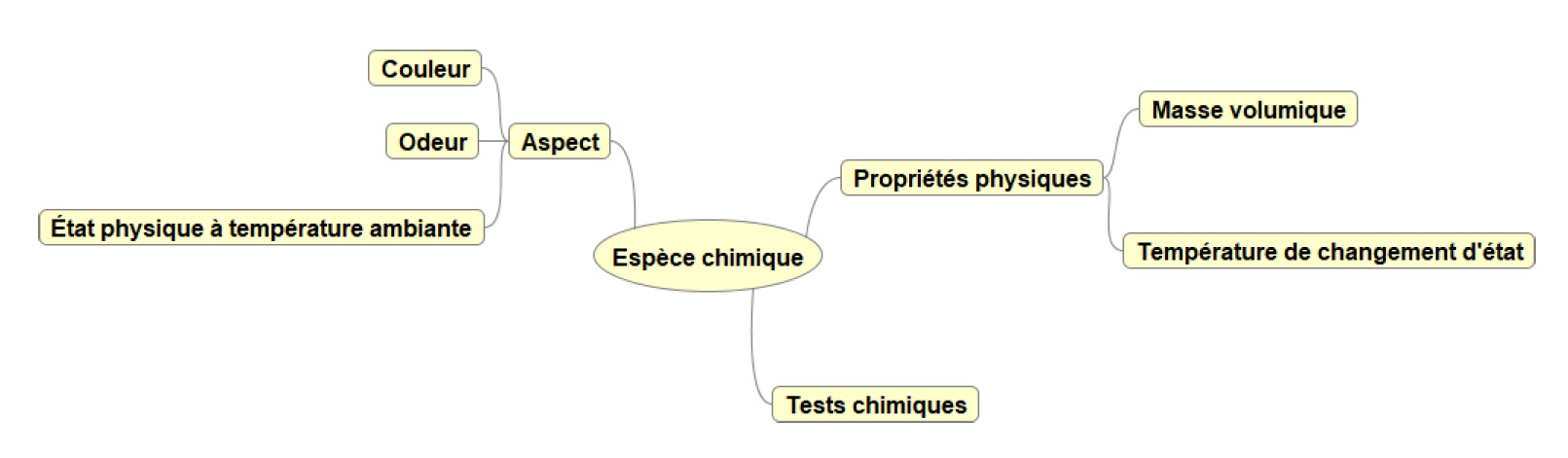
Identification d'une espèce chimique
Animation permettant de simuler le principe d'une chromatographie sur couche mince.