Stabilité des atomes
1./ Stabilité des atomes de gaz inertes :
La plupart des atomes forment des ions ou s’assemblent pour faire des molécules. Une famille d’éléments, les gaz inertes (ou gaz rares ou gaz nobles) sont inertes chimiquement : ils ne forment jamais ni d’ions, ni de molécules. On remarque qu’à part l’hélium, qui comporte 2 e– dans sa couche externe, tous les éléments de la dernière colonne ont 8 e– dans leur couche externe. C’est cette caractéristique qui explique leur grande stabilité.
He : 1s2
Ne : 1s22s22p6
Ar : 1s22s22p63s23p6
Kr : 1s22s22p63s23p64s23d104p6
etc…
2./ Règles de stabilité :
Les atomes des autres familles n’ont pas la stabilité des atomes des gaz inertes. Afin d’acquérir plus de stabilité, ils vont essayer d’acquérir la structure électronique du gaz inerte le plus proche, afin de respecter la règle du duet (2 e– dans la couche externe, soit une structure électronique en 1s2) ou la règle de l’octet (8 e– dans la couche externe, soit une structure électronique en ns2np6).
Pour acquérir la structure électronique du gaz inerte le plus proche, les atomes peuvent suivre plusieurs mécanismes. Nous allons en étudier deux : la formation d’un ion, ou la création d’une liaison covalente, afin de former une molécule.
Formation des ions monoatomiques
1./ Cas des anions :
Prenons l’exemple de l’atome de soufre (S), de numéro atomique Z = 16. Sa structure électronique est donc : 1s22s22p63s23p4.
Il y a 6 e– dans sa couche externe : un atome de soufre isolé ne respecte donc pas la règle de l’octet.
En regardant la classification périodique, on se rend compte que les deux gaz inertes qui entourent le soufre sont le néon (Ne) de numéro atomique Z = 10, et l’argon (Ar) de numéro atomique Z = 18.
L’atome de soufre a donc deux possibilités :
• Il peut perdre 6 e– pour acquérir la structure électronique du néon et former ainsi l’ion S6+.
• Il peut gagner 2 e– pour acquérir la structure électronique de l’argon et former ainsi l’ion S2–.
Le mécanisme le moins coûteux en énergie sera le deuxième, et l’atome de soufre va donc acquérir la structure électronique du gaz inerte le plus proche et former ainsi l’ion sulfure S2–.
2./ Cas des cations :
Prenons l’exemple de l’atome d’aluminium (Al), de numéro atomique Z = 13. Sa structure électronique est donc : 1s22s22p63s23p1.
Il y a 3 e– dans sa couche externe : un atome d’aluminium isolé ne respecte donc pas la règle de l’octet.
En regardant la classification périodique, on se rend compte que les deux gaz inertes qui entourent l’aluminium sont le néon (Ne) de numéro atomique Z = 10, et l’argon (Ar) de numéro atomique Z = 18.
L’atome de soufre a donc deux possibilités :
• Il peut perdre 3 e– pour acquérir la structure électronique du néon et former ainsi l’ion Al3+.
• Il peut gagner 5 e– pour acquérir la structure électronique de l’argon et former ainsi l’ion Al5–.
Le mécanisme le moins coûteux en énergie sera le premier, et l’atome d’aluminium va donc acquérir la structure électronique du gaz inerte le plus proche et former ainsi l’ion aluminium Al3+.
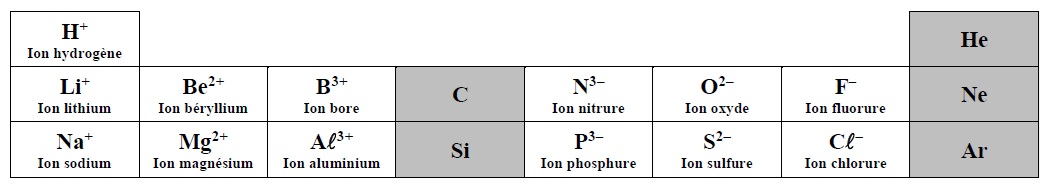
Remarques :
• Le remplissage des couches électroniques étant plus compliqué à partir de la quatrième période, on n’expliquera pas la structure des ions au-delà de la troisième ligne du tableau. (Exemple de l’atome de fer qui peut donner l’ion Fe2+ et l’ion Fe3+).
• L’atome d’hydrogène peut gagner 1 e– pour acquérir la structure électronique de l’hélium en formant l’ion H–, appelé ion hydrure. Cet ion existe et est stable. Il se rencontre beaucoup moins souvent que l’ion hydrogène H+.
Formation des molécules
1./ La liaison covalente :
Une autre méthode pour acquérir la structure électronique du gaz inerte le plus proche est la création, entre deux atomes, d’une liaison covalente.
Une liaison covalente résulte de la mise en commun de 2 e– entre deux atomes, chaque e– provenant d’un de deux atomes.
On va représenter les atomes par leur symbole et des points tout autour symbolisant les e- présents dans leur couche externe. On crée une liaison en reliant un e- d'un des atomes avec un e- du deuxième atome. Cette paire d'e- reliant deux atomes est appelée doublet liant. On s'arrête de créer des liaisons lorsque tous les atomes respectent soit la règle du duet (pour l'hydrogène), soit la règle de l'octet (pour tous les autres atomes).
Les doublets d’e– ne participant pas à une liaison chimique sont appelés doublets non liants.
Exemples :
H : 1s1, N : 1s22s22p3, O : 1s22s22p4, Cl : 1s22s22p63s23p5. Ces 4 atomes ont respectivement : 1, 5, 6 et 7 e- dans leur couche externe.
Soit la molécule de chlorure d'hydrogène, de formule HCl :
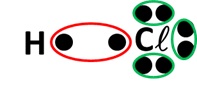
L'atome d'hydrogène va partager son unique e- avec l'atome de chlore, et l'atome de chlore va partager un de ses e- externes avec l'atome d'hydrogène, en formant une liaison covalente : les deux e- partagés appartiennent alors aux deux atomes en même temps. On peut ainsi vérifier que l'atome d'hydrogène respecte la règle du duet. L'atome de chlore, lui, respecte la règle de l'octet.
La molécule ainsi formée comprend un doublet liant (entouré en rouge sur le schéma), et les autres e- de la couche externe de l'atome de chlore vont former trois doublets non liant (entourés en vert sur le schéma).
Autre exemple : la molécule d'eau, de formule H2O :
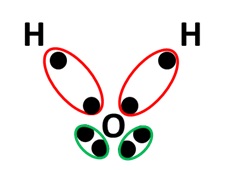
Dernier exemple : la molécule d'ammoniac, de formule NH3 :
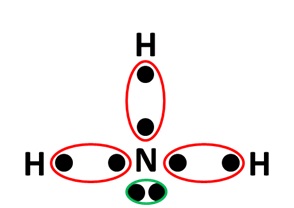
On pourra vérifier dans ces deux derniers exemples que les atomes d'hydrogène respectent tous la règle du duet, et que les autres atomes respectent tous la règle de l'octet.
A coté de ces liaisons simples, il peut exister des liaisons multiples : double ou triple : exemple des molécules de dioxygène O2 et diazote N2 :

2./ La formule de Lewis :
Pour tracer la formule de Lewis, on symbolise les doublets liants et non liants par des traits :
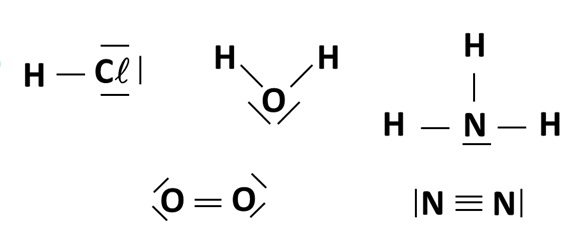
Remarques :
• Pour vérifier la validité d’une formule de Lewis, il suffit de compter les doublets autourde chaque atome : mis à part l’hydrogène qui ne doit en avoir qu’un (respect de la règle du duet), tous les autres doivente avoir 4 (respect de la règle de l’octet).
• Dans certaines molécules, la règle de l’octet n’est pas vérifiée. Nous ne nous occuperons pas de ces molécules cette année. (Ex : BeH2 ou AlH3).
3./ Les isomères :
La formule brute d’une molécule donne la composition de cette molécule, c’est-à-dire le nombre et la nature des différents atomes qui entrent dans sa composition.
La formule développée d’une molécule donne l’ordre d’enchaînement des atomes qui la constituent, en représentant par des traits les liaisons entre atomes.
La formule semi-développée est une simplification de la formule développée, où l’on ne représente pas les liaisons entre les atomes d’hydrogène et les autres atomes.
Exemple : voici les formules brute, développée et semi-développée de la molécule d’éthanol :
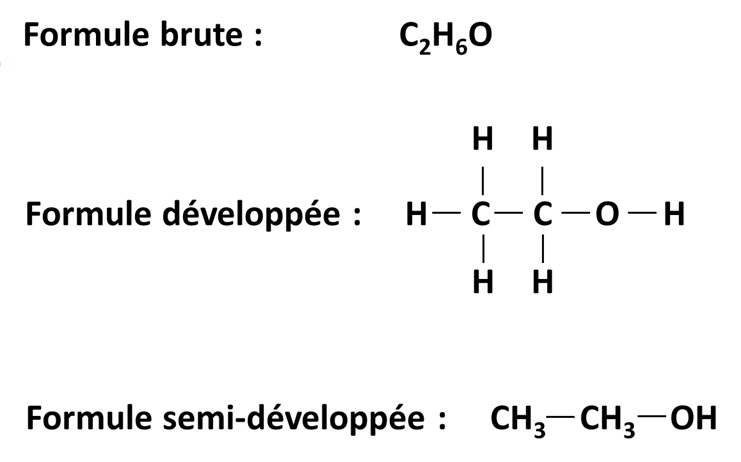
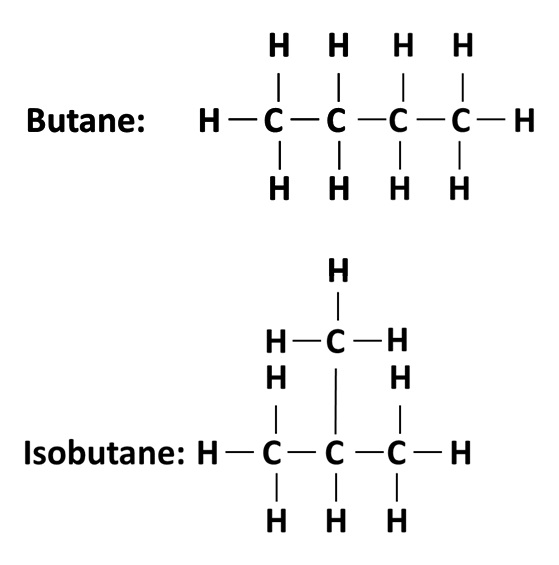
Des isomères sont des molécules qui ont la même formule brute mais des formules développées (ou semi-développées) différentes.
Exemple : voici les formules développées des molécules de butane et d’isobutane, qui ont toutes deux la même formule brute : C4H10.
4./ Notion d’énergie de liaison :
L’énergie d’une liaison est l’énergie qu’il faut apporter à une molécule afin de rompre cette liaison. Par exemple il faut une énergie d’environ 6,81 × 10–19 J, soit 4,26 eV (1 eV = 1 électron-volt = 1,6 × 10–19 J) pour rompre une liaison simple entre un atome de carbone et un atome d’hydrogène.
Inversement, lorsqu’un atome de carbone et un atome d’hydrogène créent une liaison covalente entre eux, une énergie de 6,81 × 10–19 J est dégagée, ce qui explique la stabilité accrue des molécules par rapport aux atomes isolés.